Zurück zur Homepage der Umweltstation
Iffens
zurück zur Übersicht der Projekte
zurück zum Projekt Chemie und Watt,
Themenliste
Ionenaustausch
Ein Tonboden kann viele verschiedene Formen haben. Nasser Ton ist glitschig
und kann zwischen den Fingern zerrieben werden, während trockener
Ton steinhart ist und Risse hat.
Die Eigenschaften des Tons kommen von seinem Schichtaufbau. Was der
Schichtaufbau bewirkt wollen wir uns jetzt ansehen.
Versuch 1
Quellmodell für Tonböden
Geräte und Materialien
2 gleich große Bücher
Schale
Wasser
Arbeitsanleitung
Bücher sind im allgemeinen trocken. Was passiert, wenn sich ein
Buch mit Feuchtigkeit vollsaugt ?
Nehme ein altes Buch, das du nicht mehr benötigst, gib es in eine
Schale mit Wasser, so daß es vollständig bedeckt ist.
An welchen Stellen beginnt sich das Buch mit Wasser vollzusaugen
?
Wo kommt das Wasser als letztes an ?
Lege das nasse Buch neben das trockene und vergleiche die beiden.
Miß mit einem Meßstab die Dicke der beiden Bücher.
An welchen Stellen beginnt das Buch zu trocknen ?
Wo bleibt das Wasser am längsten ?
Überlege Dir, wo das Restwasser im Boden gespeichert wird,
ist es gut für Pflanzen zugänglich ?
Die Beweglichkeit der Tonschichten kannst Du Dir mit einem Kartenstapel
veranschaulichen.
Nimm einen Satz alter, benutzter Spielkarten und einen neuen.
Die neuen Karten gleiten gut übereinander. Dieser Zustand entspricht
Tonpartikeln mit einer Wasserschicht.
Mit den benutzten Spielkarten geht das gleiten nicht mehr so gut. Die
Karten kleben stärker aneinander.
Überlege Dir bei welcher Luftfeuchtigkeit Bodenpartikel eine
Wasserschicht besitzen.
Eine weitere Eigenschaft von Ton ist seine Volumenänderung bei
Feuchtigkeit, bzw. Trockenheit. Der folgende Versuch soll eine Vorstellung
davon geben.
Versuch 2
Polyederrisse
Geräte und Materialien
Schlick (sehr tonhaltig)
weite, flache Glas- oder Metallschale
Trockenofen
Arbeitsanleitung
Beim Austrocknen können in Böden Risse entstehen.
Als extremes Beispiel beobachten wir die Rissbildung in sehr tonhaltigem
Material.
Besorge Dir einen kleinen Eimer voll weichem Schlick. Fülle den
sandarmen Schlick etwa zwei Finger breit in eine Schale.
Lege die Schale in einen Trockenschrank oder auf einem Heizkörper
bis der Schlick völlig trocken ist (das kann einige Tage dauern).
Beobachte ab und zu was passiert.
Um das Volumen der Polyederrisse abzuschätzen kannst Du die Schale
so weit mit Wasser füllen bis der getrocknete Boden damit bedeckt
ist.
Diese Wassermenge ersetzt das geschrumpfte Volumen.
Gieße das Wasser dann gleich in ein Messgefäß ab und
bestimme so in ml das entstandene Luftvolumen.
Die Risse sind nicht nur auf die Oberflächen beschränkt.
Beobachte was passiert, wenn der Boden mit Wasser getränkt wird.
Nachdem Du gesehen hast, wie der Wassergehalt des Bodens die Form und
das Bodengefüge beeinflussen kann wollen wir einmal sehen, welchen
Gewichtsanteil das Wasser in einem wassergesättigten Boden hat.
Versuch 3
Trockengewicht von Schlickböden
Geräte und Materialien
Waage
Schlick
Trockenschrank
Arbeitsanleitung
Gib etwa drei Hand voll des frischen Schlickboden in ein Glas-oder
Blechgefäß, das Du vorher gewogen hast.
Wiege das Gefäß nun mit dem Schlick und notiere das Gewicht.
Trockne den Boden in einem Trockenschrank oder Ofen bei etwa 100 Grad.
Falls das nicht möglich ist kannst Du den Boden auch einige Tage
an einen sonnigen, trockenen Ort oder auf einen Heizkörper stellen.
Wiege den Boden erneut wenn er trocken ist und berechne die Wassermenge
die aus dem Boden verdunstet ist.
Wiederhole den Versuch drei Mal und berechne den mittleren Wassergehalt
der drei Proben.
|
1.Probe |
2.Probe |
3.Probe |
Mittelwert |
| Einwaage in g |
|
|
|
|
| Trockengewicht in g |
|
|
|
|
| Wassergehalt in g |
|
|
|
|
| Wassergehalt in % |
|
|
|
|
Das Bodenwasser ist sehr wichtig für Pflanzen. Wie kommt es aber
das Wasser nicht, der Schwerkraft folgend, im Boden versickert?
Wenn Du einen dünnen Strohhalm oder eine Glaskapillare einen Becher
Wasser hälst wirst Du feststellen, daß in der Kapillare das
Wasser nach oben steigt.
Pflanzen nützen diesen Effekt, da sie in ihren Stengeln kleine
Kapillargefäße besitzen. Der Wassertransport erfolgt durch die
Verdunstung in den Blättern, hier wird den Kapillaren Wasser entzogen.
Mit einem einfachen Modell wird sichtbar, das so große Mengen
Wasser transportiert werden können.
Versuch 4
Kapillarwirkung
Geräte und Materialien
ein Taschentuch oder ein Stück Küchenrolle
2 Tassen
Wasser
Arbeitsanleitung
Wasser kann im Boden in großen Mengen entgegen der Schwerkraft
transportiert werden und von Pflanzen aufgenommen werden. Dies geschieht
in Kapillaren.
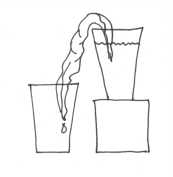
Stelle die Tassen so nebeneinander, daß eine von beiden etwas
höher als die andere steht. Fülle die höherstehende Tasse
mit Wasser.
Verteile das Taschentuch so auf beide Tassen, dass es das Wasser in
der oberen Tasse berührt und in der unteren Tasse tiefer hängt
(siehe Skizze).
Beobachte was geschieht.
Gehst Du nach einem starken Regen auf einem Sandstrand spazieren, dann
ist der Sand nur feucht, während Du auf einem Marschboden durch Pfützen
und Schlamm läufst.
Das liegt an der unterschiedlichen Wasserspeicherfähigkeit und
dem unterschiedlich schnell ablaufendem Wasser.
Versuch 5
Wasserdurchlässigkeit, -kapazität
Geräte und Materialien
1,5 L PET-Flaschen
Watte
je 500g Bodenprobe (z.B. Sand, Torf, Oberboden(knapp unterhalb der
Wurzelschicht), Unterboden (ca.30-40cm Tiefe)
200ml Bechergläser
Arbeitsanleitung
Trockne die Bodenproben in einem Trockenschrank, bei 105°C oder
lasse sie an der Luft trocken werden.
Säge den Boden der PET-Flaschen ab, bohre ein etwa 3mm dickes
Loch in den Deckel und stecke ein Stück Watte in den Flaschenhals.
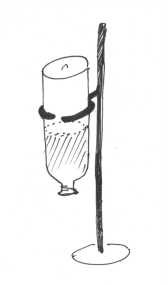
Befestige die Flaschen so an einem Stativ, das sie mit dem Kopf nach
unten über einem Becherglas hängen (vergleiche Skizze).
Vergleiche die Durchflußgeschwindigkeiten der Flaschen, indem
Du in alle Flaschen die gleiche Menge Wasser füllst und wartest bis
das Wasser durchgeflossen ist.
Achte darauf, das Du nur Flaschen verwendest, deren Durchflussgeschwindigkeit
ähnlich ist.
Als Alternative zu den durchbohrten Deckeln kannst du auch Korken mit
einem abgeschrägten Ende verwenden. Hier kannst Du den Durchfluss
variieren, je nachdem wie weit der Korken in der Flasche steckt.
Siebe alle (außer den Torf) Bodenproben durch ein gleich grosses
Sieb.
Falls die Tonböden zu grob sind kannst Du sie mit einem Mörser
zerkleinern.
Wiege jeweils 500g von jeder Bodenprobe ab und fülle sie in die
Flaschen.
Gib jetzt zu jeder Bodenprobe schrittweise jeweils 50ml Wasser.
Warte bis das Wasser versickert ist und gib dann noch einmal 50ml Wasser
dazu. Notiere die Wassermenge, die Du zugegeben hast, wenn das Wasser beginnt
aus der Flasche zu tropfen.
Die zugegebene Wassermenge entspricht der Wasserkapazität des
Bodens.
Nachdem das Wasser abgetropft ist hast Du einen wassergesättigten
Bodenkörper.
Jetzt gibst Du noch einmal 50ml Wasser auf den Boden.
Notiere die Zeit die das Wasser benötigt um den Boden zu passieren.
Bei tonigen Böden kann dies sehr lange dauern, daher kannst du
auch die Wassermenge bestimmen, die nach einer oder zwei Stunden durchgeflossen
ist und damit die Gesamtzeit abschätzen.
Ist das Wasser das jetzt abfließt das gleiche, das Du oben
hineingeschüttet hast ?
Beschreibe die Unterschiede zwischen den Bodenarten ?
Verwende in einem neuen Versuch Bodenproben, die Du nur getrocknet
und nicht zerkleinert hast.
Wie ändert sich das Ergebnis ? Woran liegt das ?
Die Düngung der Äcker im Winter macht Sinn, da die Nährstoffe,
die dem Boden zugeführt werden, gespeichert werden können. Dies
ist möglich da die Nährstoffe als Ionen beigegeben werden, die
an den Bodenpartikel adsorbieren können.
Im folgenden wollen wir die unterschiedlichen Speicherfähigkeiten
der Böden untersuchen.
Versuch 6
Abschätzung der Ionenaustauschkapazität
Geräte und Materialien
1,5 L PET-Flaschen
Watte
je 500g Bodenprobe (z.B. Sand, Torf, Oberboden(knapp unterhalb der
Wurzelschicht), Unterboden (ca.30-40cm Tiefe)
200ml Bechergläser
Leitfähigkeitsmessgerät
Kochsalz
Durchflussmethode Diesen Versuch kannst Du zusammen mit dem
Wasserkapazitätsversuch durchführen.

Trockne die Bodenproben in einem Trockenschrank, bei 105°C oder
lasse sie an der Luft trocken werden.
Säge den Boden der PET-Flaschen ab, bohre ein etwa 3mm dickes
Loch in den Deckel und stecke ein Stück Watte in den Flaschenhals.
Befestige die Flaschen so an einem Stativ, das sie mit dem Kopf nach
unten über einem Becherglas hängen (vergleiche Skizze).
Vergleiche die Durchflußgeschwindigkeiten der Flaschen, indem
Du in alle Flaschen die gleiche Menge Wasser füllst und wartest bis
das Wasser durchgeflossen ist.
Achte darauf, das Du nur Flaschen verwendest, deren Durchflußgeschwindigkeit
ähnlich ist.
Als Alternative zu den durchbohrten Deckeln kannst du auch Korken mit
einem abgeschrägten Ende verwenden. Hier kannst Du den Durchfluss
variieren, je nachdem wie weit der Korken in der Flasche steckt.
Siebe alle (außer den Torf) Bodenproben durch ein gleich grosses
Sieb.
Falls die Tonböden zu grob sind kannst Du sie mit einem Mörser
zerkleinern.
Messe die Leitfähigkeit des Wassers, das Du auf die Böden
gießt und des Wassers, das die Böden durchflossen hat und notiere
das Ergebnis.
Gib solange Wasser auf die Böden bis die im Durchflußwasser
gemessene Leitfähigkeit sich nicht mehr von der des zugegebenen Wassers
unterscheidet.
Vergleiche die Anzahl der Durchgänge, die für die verschiedenen
Böden nötig sind.
Wo sind die meisten Nährstoffe vorhanden ?
Jetzt versuchen wir abzuschätzen, wie viele Ionen die verschiedenen
Böden adsorbieren können.
Stelle eine 0,5 M NaCl-Lösung (entspricht etwa dem mittleren Salzgehalt
des Seewassers) her.
Messe die Leitfähigkeit der Lösung und notiere das Ergebnis.
Gib die Lösung in jeweils 100ml Portionen auf die Bodenproben.
Messe nach dem Durchfluß die Leitfähigkeit und trage den
Wert in eine Tabelle ein.
Gib solange von der NaCl-Lösung zu bis die Leitfähigkeit
im Durchflußwasser der des Salzwassers entspricht.
Leitfähigkeit von
|
Sandboden |
Oberboden |
Unterboden |
Torfboden |
|
|
| +100 ml |
|
|
|
|
|
|
| +100 ml |
|
|
|
|
|
|
| +100 ml |
|
|
|
|
|
|
| +100 ml |
|
|
|
|
|
|
| +100 ml |
|
|
|
|
|
|
| +100 ml |
|
|
|
|
|
|
| Summe |
|
|
|
|
|
|
Für die Abschätzung benötigst Du eine Messreihe mit verschiedenen
NaCl-Konzentrationen.
Stelle vier NaCl-Lösungen mit den Konzentrationen 0,01, 0,05,
0,1 und 0,25 her.
|
0,05M NaCl |
0,1M NaCl |
0,2M NaCl |
0,4M NaCl |
0,5M NaCl |
| Leitfähigkeit in mS |
|
|
|
|
|
Messe von jeder Lösung die Leitfähigkeit und notiere das Ergebnis.
Erstelle einen Graphen indem Du die Leitfähigkeit gegen die Konzentration
aufträgst.
Um die Konzentration abzuschätzen musst Du die Gesamtleitfähigkeit
der adsorbierten Ionen berechnen. Trage in die Tabelle für jeden Durchlauf
die Differenzen zwischen der zugegebenen und der abgeflossenen Leitfähigkeit
ein. Addiere dann diese Werte für jeden Boden. Suche im Graphen die
zu diesem Leitfähigkeitswert gehörende Konzentration. Diese entspricht
einer groben Abschätzung der adsorbierten Ionenkonzentration.
|
Anzahl Durchläufe x Leitfähigkeit von 0.5M NaCl - Leitfähigkeitssumme
Sandboden |
Anzahl Durchläufe x Leitfähigkeit von 0.5M NaCl - Leitfähigkeitssumme
Oberboden |
Anzahl Durchläufe x Leitfähigkeit von 0.5M NaCl - Leitfähigkeitssumme
Unterboden |
Anzahl Durchläufe x Leitfähigkeit von 0.5M NaCl - Leitfähigkeitssumme
Torfboden |
| Leitfähigkeit der adsorbierten Ionen |
|
|
|
|
|
|
|
|
|
Vergleiche die Adsorbtionsfähigkeit der Böden.
Batch-Methode
Geräte und Materialien
Magnetrührer
500 ml Becherglas
dest. Wasser
Bodenproben
Stativ
Diese Methode ist etwas weniger zeitaufwendig als die vorhergehende.
Gebe zu 50g einer Bodenprobe 300 ml dest. Wasser und einen Rührfisch.
Stelle den Behälter auf den Magnetrührer und befestige den
Leitfähigkeitsmesser mit einem Stativ so, daß er in die Lösung
taucht ohne den Rührfisch zu behindern.
Stelle den Magnetrührer an und beobachte die Leitfähigkeitsänderung,
wobei du, falls vorhanden, einen y-t-Schreiber verwenden kannst.
Unterscheiden sich die Maximalwerte und die Geschwindigkeit der
Leitfähigkeitsänderung der Bodenproben ?
Lasse die Lösung einen Tag stehen und messe dann erneut die
Leitfähigkeit. Gibt es unterschiede zum Vortag ? Wenn ja, woher stammen
diese ?
Mehrwertige Ionen von Schwermetallen wirken in grossen Mengen schädlich
für die Vegetation und im Trinkwasser nicht erwünscht.
Mit einem einfachen Versuch kannst Du Dir eine Vorstellung davon machen,
welche Böden diese Ionen anreichern und somit als Filter dienen.
Versuch 7
Eisenadsorption
Geräte und Materialien
Bodenproben (z.B Sand und Tonboden)
FeCl3x6H2O-Lösung
2 500ml Bechergläser
Pipette
Reagenzgläser
Kaliumthiocyanat (5%)
HCl (20%)
dem. Wasser
Magnetrührer
Magnetfisch
Arbeitsanleitung
Gebe 2g FeCl3x6H2O auf 500ml destilliertes Wasser.
Fülle nach dem Schema in der Tabelle ein 500ml Becherglas mit
Boden, FeCl3x6H2O-Lösung und dem. Wasser. Die
Zahlen sollen nur als erste Näherung dienen, Du kannst sie später
noch je nach Bedarf abändern.
|
Bodenprobe in g |
FeCl3*6H2O-Lösung in ml |
dem. Wasser in ml |
| Sand |
100 |
50 |
250 |
| Ton |
15 |
300 |
- |
Stelle von der FeCl3-Lösung , die Du zugibst, eine Referenzlösung
her, indem Du 5ml der Lösung und 1ml KSCN-Lösung in ein Reagenzglas
gibst. Die Lösung färbt sich blutrot.
Gib nun noch den Magnetfisch in die Lösung und stelle das Ganze
auf den Magnetrührer.
Lasse sie Lösung etwa eine Stunde rühren.
Warte bis der Boden abgesetzt hat und gib dann mit der Pipette 5ml
der Lösung in ein Reagenzglas.
Gib jetzt noch 1ml KSCN dazu. Vergleiche die Rotfärbung mit der
Referenzlösung.
Die adsobierten Eisenionen können wieder in Lösung gebracht
werden, indem ein Überschuß an H3O+ zugegeben
wird.
Um das zu erreichen gibst Du jetzt 5ml von 20% HCl in das Becherglas
und lässt die Lösung noch eine Stunde rühren.
Nach der Stunde gibst Du wieder 5ml Lösung mit 1ml KSCN in ein
Reagenzglas und vergleichst die Färbung mit der Referenzlösung.
Stimmt die Farbe noch nicht überein, dann gibst Du noch einmal
5ml HCl zu und wiederholst den ganzen Vorgang.
Vergleiche die Färbungen für jede Bodenart.
Warum sind die Mengen Boden für Sand und Ton so unterschiedlich?
Welchen Einfluß hat der saure Regen auf die Filterwirkung
der Böden ?
Zurück zur Homepage der Umweltstation
Iffens
zurück zur Übersicht der Projekte
zurück zum Projekt Chemie und Watt,
Themenliste

